- 1 高校采購信息
- 21 科技成果項目
- 0 創新創業項目
- 0 高校項目需求
細胞微泡特異標記探針
(物質科學與信息技術研究院)細胞微泡(MV)作為細胞間通訊與物質交換的重要載體,在疾病診斷和藥物遞送等領域有著廣闊的應用前景。因此,深入探究MV的生物學過程對闡明其生理和病理功能具有重要意義。然而,由于缺乏特異性標記方法,研究人員對MV的產生、分泌以及生理學作用依舊不明晰。安徽大學的張忠平/張瑞龍/耿軍龍研究團隊成功開發了一系列探針IC-Cn(n為烷基側鏈的碳原子數),實現了對MV的特異性標記,并應用于對MV及相關細胞器的原位成像。
基于MV的疏水膜環境與細胞膜、外泌體和其他細胞器的差異,通過工程化吲哚-香豆素陽離子熒光探針的疏水側鏈長度,精細調節探針的疏水性,制備了一系列熒光探針(實現了對不同亞細胞結構(MV,線粒體,內質網,外泌體和細胞膜等)的靶向。其中,低親脂性探針IC-C1,IC-C2和IC-C3(0.57 ≤ clogP ≤ 0.83)可以特異性的標記MV;中等親脂性探針IC-C3,IC-C4和IC-C5(1.10 ≤ clogP ≤ 1.97)可以同時靶向MV和線粒體,并具有可區分的熒光壽命;高親脂性的探針會染色細胞中的內質網及細胞膜。

圖1. 探針的設計及其在細胞中的定位
利用IC-C1對MV的高特異性,研究團隊在細胞中對MV進行了原位成像,觀察到MV從細胞膜上的產生、其依賴偽足的運動以及細胞內外MV的融合與分裂過程。
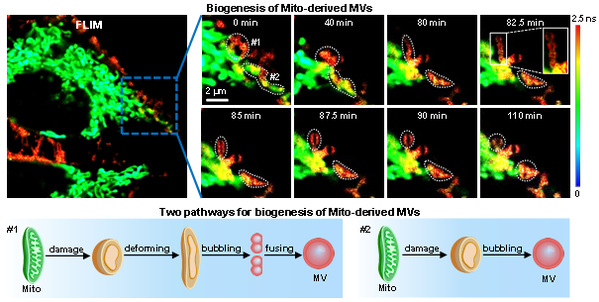
圖2. IC-C1用于監測MV動力學的原位成像
IC-C4可以同時標記MV和線粒體并具有可區分的熒光壽命。研究人員利用這一特性,原位監測了線粒體衍生MV的生物發生及其分泌過程,而且發現了部分線粒體衍生MV可以與溶酶體融合以清除受損的線粒體,揭示了一種除線粒體自噬以外的維持線粒體穩態新途徑。
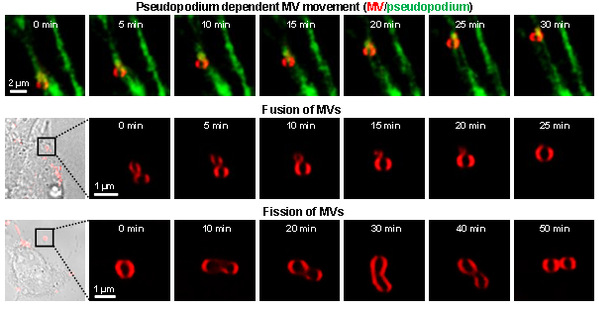
圖3. IC-C4用于監測MV與線粒體相互作用的原位成像
這項工作克服了以往MV標記所面臨的特異性差和無法進行原位成像的缺點,深入研究了MV的組成、產生、分泌和功能。不僅為MV生理學提供了新的見解,還啟發了細胞研究中用于特異性標記探針的設計策略。相關工作以Lipophilicity Modulation of Fluorescent Probes for In Situ Imaging of Cellular Microvesicle Dynamics為題發表在化學頂級期刊《Journal of the American Chemical Society》(org/10.1021/jacs.4c13516)上。安徽大學物質科學與信息技術研究院2022級博士黃威為論文的第一作者,張瑞龍副教授和耿軍龍教授為論文的共同通訊作者。

掃碼關注,查看更多科技成果