在抗擊癌癥的征途中,腫瘤微環(huán)境(TME)被認(rèn)為是腫瘤生長(zhǎng)、免疫逃逸和治療耐藥的重要“避風(fēng)港”。其中,腫瘤相關(guān)巨噬細(xì)胞(TAMs)因在免疫抑制、腫瘤促進(jìn)和治療耐藥中的獨(dú)特角色,成為當(dāng)前癌癥免疫治療的研究熱點(diǎn)。然而,如何在體內(nèi)高效且精準(zhǔn)地靶向巨噬細(xì)胞并編輯其基因,一直是科學(xué)界面臨的技術(shù)難題。
2025年1月15日,浙江大學(xué)藥學(xué)院/良渚實(shí)驗(yàn)室平淵團(tuán)隊(duì)在Science Translational Medicine雜志發(fā)表題為“Macrophage-specific in vivo RNA editing by anti-inflammatory polymeric formulation promotes phagocytosis and tumor immunity in mice”的研究論文,提出了一種基于聚β-氨基酯(PBAE)遞送系統(tǒng)和CasRx RNA編輯技術(shù)的巨噬細(xì)胞特異性編輯平臺(tái)(MAGE),該研究通過(guò)靶向巨噬細(xì)胞的RNA編輯技術(shù),有效破壞“Don’t Eat Me”信號(hào)通路,增強(qiáng)巨噬細(xì)胞吞噬能力,從而逆轉(zhuǎn)免疫抑制微環(huán)境。
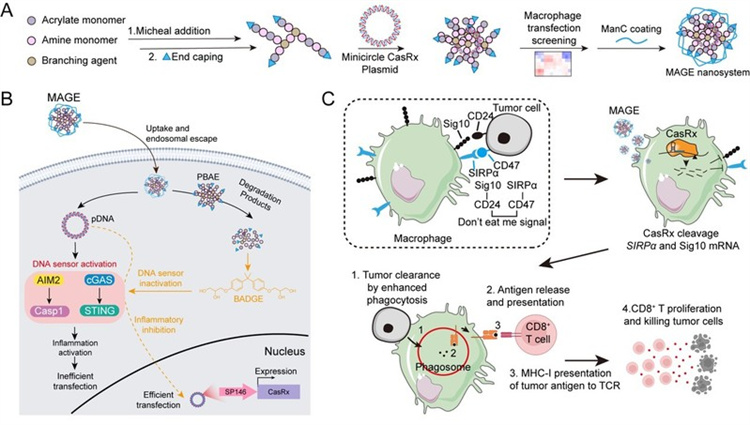
圖1. 基于PBAE構(gòu)建的巨噬細(xì)胞靶向RNA編輯遞送系統(tǒng)(MAGE)的構(gòu)建和應(yīng)用示意圖
巨噬細(xì)胞在腫瘤免疫治療中具有雙重作用。一方面,它們能夠通過(guò)吞噬腫瘤細(xì)胞發(fā)揮抗腫瘤作用;另一方面,腫瘤相關(guān)巨噬細(xì)胞(TAMs)通常在腫瘤微環(huán)境中被重新編程為促腫瘤表型。近年來(lái),“不要吃我”(Don't eat me)信號(hào),如CD47-SIRPα和CD24-Sig10軸,被證明是腫瘤細(xì)胞逃避免疫系統(tǒng)的重要機(jī)制。然而,抗體阻斷這些信號(hào)的策略往往因?yàn)樘禺愋圆蛔銓?dǎo)致副作用較多。相較之下,通過(guò)基因編輯技術(shù)直接靶向巨噬細(xì)胞表達(dá)的SIRPα和Sig10可能是一種更為精準(zhǔn)的解決方案。
但巨噬細(xì)胞在基因遞送中存在兩個(gè)主要挑戰(zhàn):外源DNA易被降解:巨噬細(xì)胞具有強(qiáng)大的核酸傳感機(jī)制(如AIM2和cGAS-STING通路),能快速識(shí)別并降解外源DNA,導(dǎo)致轉(zhuǎn)染失敗。炎癥反應(yīng)強(qiáng)烈:巨噬細(xì)胞暴露于外源核酸時(shí),往往伴隨著大量炎性因子的釋放,這不僅限制了基因編輯的效率,還可能破壞免疫微環(huán)境。基于此,開(kāi)發(fā)一種既高效又低炎癥反應(yīng)的巨噬細(xì)胞基因遞送工具顯得尤為重要。

圖2. 巨噬細(xì)胞轉(zhuǎn)染機(jī)制研究
這一技術(shù)的核心在于團(tuán)隊(duì)開(kāi)發(fā)的聚β-氨基酯(PBAE)遞送工具(Fig.1)。通過(guò)對(duì)123種PBAE聚合物的篩選,研究者發(fā)現(xiàn)四臂分支結(jié)構(gòu)的PBAE29在巨噬細(xì)胞轉(zhuǎn)染中表現(xiàn)出顯著的優(yōu)勢(shì),與傳統(tǒng)遞送方式相比,PBAE29能夠顯著提高轉(zhuǎn)染效率并顯著減少炎癥反應(yīng)。圖像與流式細(xì)胞術(shù)數(shù)據(jù)顯示,PBAE29遞送效率最高且炎癥因子的釋放最低(如IFN-β和IL-6)。此外,PBAE29通過(guò)結(jié)合Minicircle微環(huán)質(zhì)粒進(jìn)一步降低了炎性因子水平,優(yōu)化了轉(zhuǎn)染效率。研究還通過(guò)實(shí)驗(yàn)驗(yàn)證了PBAE29能有效避免與AIM2通路的過(guò)度激活,從而降低細(xì)胞死亡風(fēng)險(xiǎn)。
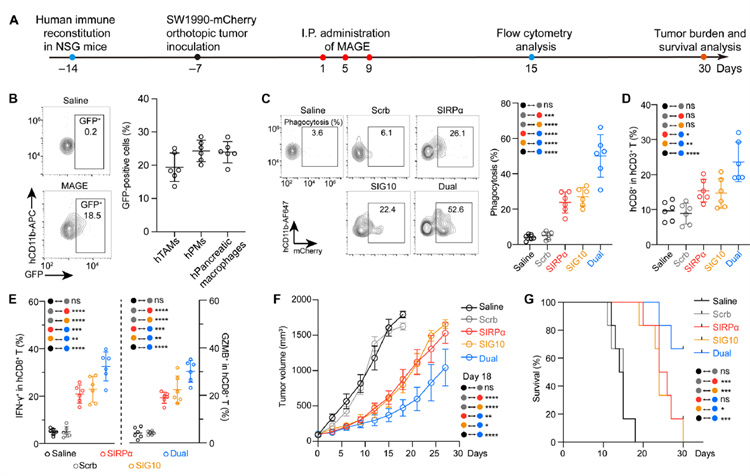
圖3. MAGE系統(tǒng)用于人源化小鼠的治療
這一突破性成果顯示,MAGE系統(tǒng)不僅能夠精準(zhǔn)靶向巨噬細(xì)胞,降低炎癥反應(yīng),還通過(guò)CasRx RNA編輯工具抑制巨噬細(xì)胞表面的“Don’t Eat Me”信號(hào)(SIRPα和Sig10)。這些編輯后的巨噬細(xì)胞吞噬能力大幅提升,直接破壞腫瘤微環(huán)境的免疫抑制特性,并通過(guò)抗原呈遞激活T細(xì)胞,誘導(dǎo)持久的抗腫瘤免疫反應(yīng)。
浙江大學(xué)藥學(xué)院畢業(yè)生陳宇軒博士及陳小紅博士為該論文共同第一作者,浙江大學(xué)藥學(xué)院/良渚實(shí)驗(yàn)室平淵教授為該論文獨(dú)立通訊作者,主要合作者為中國(guó)科學(xué)院過(guò)程工程研究所魏煒研究員。






.jpg)