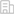抗壞血酸(H2A,又稱維生素C)是一種廣泛存在于各種食物中的維生素,它是一種抗氧化劑,可幫助保護細胞免受自由基的影響。近年來,抗壞血酸也被作為一種高效的促氧化劑,用于癌癥治療。然而,抗壞血酸“抗氧化”和“促氧化”作用相互“矛盾”,人們尚不清楚該生物醫學功能雙面性背后的分子機制,阻礙了抗壞血酸在生物醫學中的應用。
由于在原子水平上具有與天然酶相似的催化中心,單原子納米酶被視為天然酶的模擬物,被廣泛應用于生物傳感、藥物相互作用和疾病治療等領域。鑒于此,近日,東南大學張袁健教授課題組提出使用Fe-N-C納米酶作為鐵蛋白模擬物探索抗壞血酸催化氧化反應的機制。
該團隊發現Fe-N-C納米酶是一種多相催化劑,具有N-C和Fe-Nx兩種活性位點,Fe-N-C中的Fe-Nx位點主要通過結合態中間體催化抗壞血酸氧化和四電子氧還原,同時,少量N-C位點催化二電子氧還原,催化過程中產生痕量超氧陰離子并誘導Fe-N-C中不穩定的Fe-Nx游離為Fe離子。進而,經N-C位點催化產生的過氧化氫與游離的Fe離子形成芬頓體系,衍生出一個新的四電子氧還原過程。更為重要的是,當游離的Fe離子遠離催化劑時,由于抗壞血酸催化氧化過程中Fe-Nx活性位點含量的下降,更多的N-C活性位點被激活,從而直接導致過氧化氫產率上升。該研究率先發現Fe-N-C納米酶催化抗壞血酸氧化過程中的Fe離子的析出現象,并揭示了一個新的氧氣還原途徑,對理解抗壞血酸促氧化效應用于清除癌細胞提供了一個新思路。

Fe-N-C納米酶催化抗壞血酸氧化的三種路徑(圖片來自Angew. Chem. Int. Ed.)
東南大學化學化工學院的碩士生曹栩雯和博士生朱彩霞為本工作共同第一作者,通訊作者為化學化工學院張袁健教授和醫學院沈艷飛教授,東南大學為該工作的唯一完成單位,該工作得到了國家自然科學基金的資助。